前次IPO已注册生效,最终因注册批文到期未发而倒在上市门前的西安新通药物研究股份有限公司(以下简称“新通药物”),如今再次向科创板发起冲击。近期,公司科创板IPO获得受理。与前次IPO相比,此次申报,新通药物已有核心产品上市。由于核心产品上市不久,新通药物尚未实现盈利。公司两次闯关科创板均系按第五套上市标准申报。对比前次IPO,新通药物募投项目未发生变化,但募资额出现缩水,由12.79亿元下降至9亿元。此外,作为一家尚未实现盈利的创新药企,新通药物研发费用于2024年出现锐减。新通药物此次重走科创板IPO之路,能否最终实现上市,尚是未知数。
二度IPO
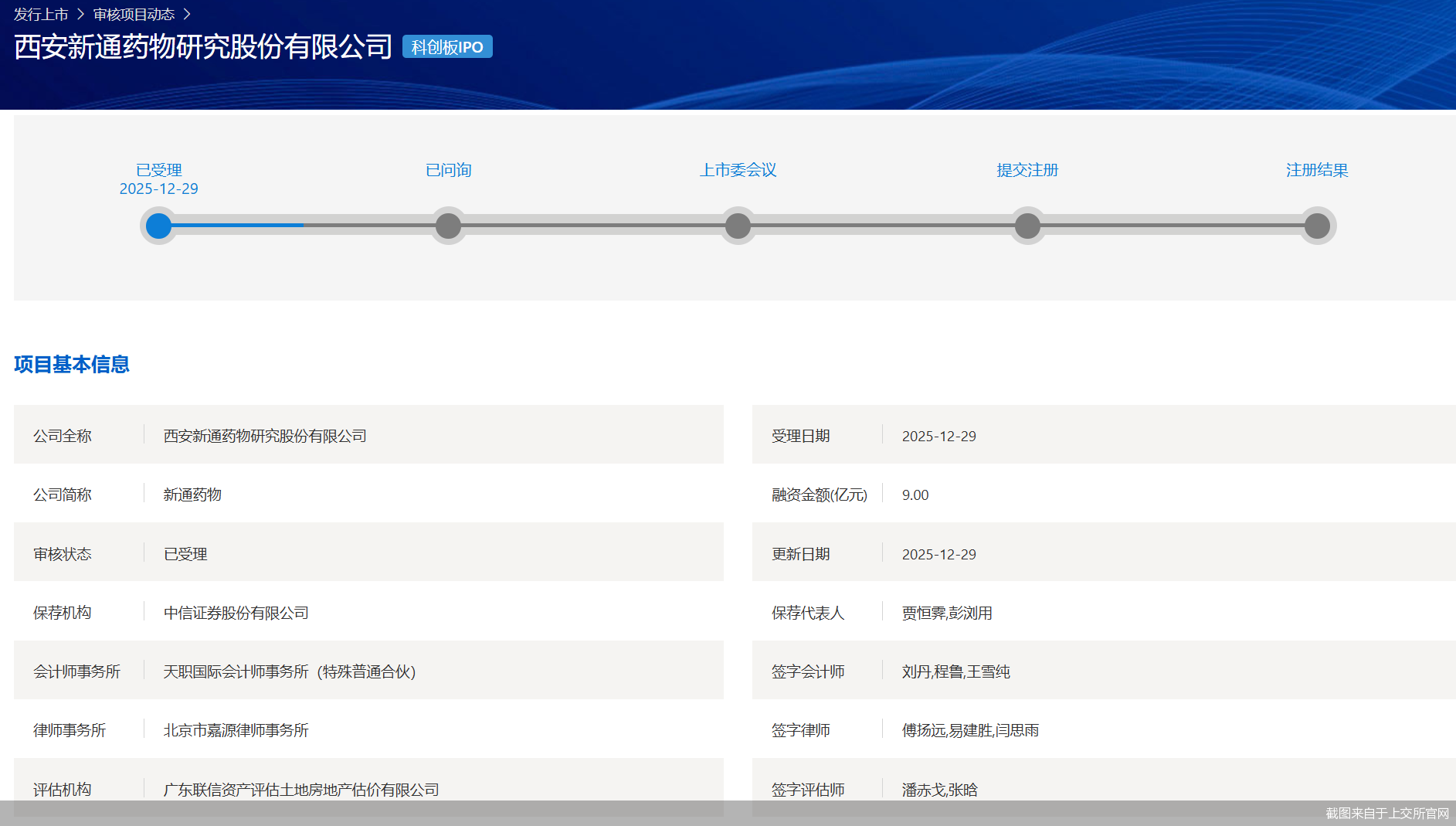
上交所官网显示,近期,新通药物科创板IPO已获受理。
招股书显示,新通药物是一家专注药物研发20余年的高新技术企业,聚焦于乙肝、代谢功能障碍相关脂肪性肝炎及肝癌等重大肝病领域的药物开发,致力于研发具有自主知识产权、安全有效、以临床价值为导向的创新药物,力求填补肝病领域未被满足的临床需求,现已快速发展成为一家具备竞争力的肝病新药开发企业。
值得一提的是,这是新通药物第二次闯关科创板。回顾新通药物前次IPO之路,2021年12月6日,新通药物科创板IPO获得受理。2022年12月12日,新通药物获得上会机会,不过首次上会遭到暂缓审议。2023年1月12日,新通药物再度获得上会机会,此次上会获得通过。同年4月13日,新通药物提交注册,并于同年4月25日注册生效。不过,注册生效后,新通药物未能成功发行,最终因注册批复失效而倒在上市门口。
两次闯关科创板,新通药物均符合并适用《上海证券交易所科创板股票上市规则》第2.1.2条规定的上市标准中的第(五)项标准:“预计市值不低于人民币40亿元,主要业务或产品需经国家有关部门批准,市场空间大,目前已取得阶段性成果。医药行业企业需至少有一项核心产品获准开展二期临床试验,其他符合科创板定位的企业需具备明显的技术优势并满足相应条件。”
截至目前,新通药物尚未实现盈利。2022—2024年以及2025年上半年,新通药物归属净利润分别为-5387.1万元、-6229.25万元、-7935.55万元和-1320.36万元。截至2025年6月末,公司合并报表层面累计未弥补亏损为34675.87万元,公司尚未盈利且存在累计未弥补亏损。
科方得咨询机构负责人张新原向北京商报记者表示,对于医药行业来说,科创板第五套上市标准的核心意义在于为研发周期长、投入大的创新药企开辟融资通道。该标准主要关注企业的技术先进性和研发能力,而非短期财务指标,适合处于关键研发阶段的生物医药企业。这类企业通常已完成核心产品概念验证,但尚未实现盈利,需要持续资金支持完成临床试验和上市审批。
募资额减少至9亿元
与前次IPO相比,新通药物募资额出现减少。
招股书显示,此次科创板IPO,新通药物拟募集资金9亿元,投向新药研发项目、创新药物产业化生产基地建设项目以及补充流动资金项目,拟分别投入募资额5亿元、2亿元、2亿元。
根据新通药物前次IPO注册稿,新通药物前次IPO拟募集资金12.79亿元。前次IPO募投项目与此次IPO相同,拟投入募资额分别为8.99亿元、1.8亿元、2亿元。
与前次IPO相比,新药研发项目拟投入募资额出现明显下降,创新药物产业化生产基地建设项目拟投入募资额略有增长。
具体来看,根据新通药物招股书,此次新药研发项目募集资金将用于四个核心药物,分别为靶向抗肝癌药物注射用MB07133、靶向抗乙肝药物富马酸海普诺福韦(HTS)、抗乙肝病毒核衣壳蛋白抑制剂XTYW001和治疗代谢功能障碍相关脂肪性肝炎药物XTYW007共4个创新药物,包括临床试验费用、人工费用等,从而推动产品的研发进展以及上市进度。
此外,北京商报记者注意到,前次IPO时,新通药物主要核心产品仍处于研发阶段,尚未开展商业化生产销售。此次申报,新通药物已有核心产品上市。公司核心产品肝靶向1类新药甲磺酸普雷福韦片(商品名:新舒沐)于2024年10月于中国获批上市,并于2024年12月开始销售。截至招股书签署日,公司拥有8个治疗肝病的核心产品,除了已获批上市的新舒沐外,2个产品注射用MB07133及富马酸海普诺福韦片已处于II/III期无缝连接的注册性临床试验阶段,1个产品XTYW001已完成Ia期临床试验,1个产品XTYW007已提交IND申请,3个在研肝病产品处于临床前研发阶段。
从营业收入来看,2022—2024年以及2025年上半年,新通药物营业收入分别约为110.03万元、1197.82万元、301.87万元、976.7万元。
2024年研发费用骤降
对于以科创板第五套上市标准申报上市的创新药企来说,研发能力至关重要,研发投入也是监管层在审核中关注的重要指标之一。
招股书显示,报告期内,新通药物研发费用出现明显下降。2022—2024年,新通药物研发费用分别为5323.17万元、6209.6万元、2608.41万元。2025年上半年,新通药物研发费用为1268.62万元。
北京中医药大学卫生健康法治研究与创新转化中心主任邓勇表示,创新药企的核心壁垒是研发管线,研发费用是维持其“创新属性”的生命线。研发费用持续下降,可能会面临新药研发进度放缓、核心竞争力下降等风险。不过,也需要根据公司的研发阶段具体情况具体分析。
新通药物表示,公司研发费用主要由试验费、折旧摊销费、材料费、人工费等构成。2024年公司研发费用较2023年下降57.99%,主要系试验费、折旧摊销费和材料费下降较多。
其中,公司2024年试验费较2023年下降73.17%,主要系富马酸海普诺福韦片项目完成Ic/IIb期临床试验后,于2024年与CDE就III期临床方案进行沟通交流,最终确定II/III期无缝连接的注册性临床方案于2025年下半年启动,导致2024年相关试验费下降。甲磺酸普雷福韦片于2023年5月提交上市审批,2024年10月取得批件,在此期间,公司将研发投入资本化,计入开发支出,导致相关试验费下降。
此外,报告期各期,公司研发费用中折旧摊销费下降较多,主要系MB07133相关非专利技术于2023年10月到期摊销结束;2023年5月至2024年10月,甲磺酸普雷福韦片项目相关非专利技术折旧摊销计入开发支出,导致计入研发费用的折旧摊销金额减少。
针对公司相关问题,北京商报记者向新通药物方面发去采访函,不过截至记者发稿,未收到公司回复。
北京商报记者 丁宁

本网站所有内容属北京商报社有限公司,未经许可不得转载。 商报总机:010-64101978 版权合作:010-64101871
商报地址:北京市朝阳区和平里西街21号 邮编:100013 法律顾问:北京市中同律师事务所(010-82011988)
![]()
 网上有害信息举报 违法和不良信息举报电话:010-84276691 举报邮箱:bjsb@bbtnews.com.cn
网上有害信息举报 违法和不良信息举报电话:010-84276691 举报邮箱:bjsb@bbtnews.com.cn
ICP备案编号:京ICP备08003726号-1  京公网安备11010502045556号 互联网新闻信息服务许可证11120220001号
京公网安备11010502045556号 互联网新闻信息服务许可证11120220001号